 Principles of Chemistry
Principles of Chemistry
- > Home
-
>
Historia chemii
- > Początki chemii
- > Rozwój alchemii
- > Jatrochemia
- > Badanie spalania i powietrza
- > Odkrycie i badanie gazów
- > Powstanie nowoczesnej chemii
- > Prawa chemiczne
- > Narodziny teorii atomowej
- > Elektrochemia
- > Berzelius, Hisinger, Faraday
- > Początki chemii organicznej
- > Substytucja
- > Wartościowość
- > Chemia fizyczna
- > Rozwój chemii nieorganicznej
- > Struktura atomu
-
>
Pierwiastki
- > Starożytność
- > Średniowiecze
- > Powietrze i woda
- > Analiza chemiczna
- > Halogeny
- > Elektrochemia
- > Metody spektroskopowe
- > Pierwiastki ziem rzadkich
- > Gazy szlachetne
- > Pierwiastki radioaktywne
- > Szeregi pierwiastków promieniotwórczych
- > Pierwiastki otrzymane sztucznie
- > Pierwiastki transuranowe
- > Podsumowanie
- > Układ okresowy
-
>
Mechanika falowa
- > Podstawy teoretyczne
- > Moment pędu
- > Równanie Schrodingera
- > Oscylator liniowy
- > Pole o symetrii sferycznej i pole kulombowskie
- > Spin
- > Identyczność cząstek
- > Oddziaływanie wymienne
- > Druga kwantyzacja
- > Poziomy energetyczne atomów
- > Układ okresowy
- > Atom w polu elektrycznym
- > Atom w polu magnetycznym
- > Cząsteczka dwuatomowa
- > Orto- i parawodór
- > Teoria relatywistyczna
- > Kwantowanie pola elektromagnetycznego
- > Fotony
- > Równanie Diraca
- > Cząstki i antycząstki
- > Atom i cząsteczka
-
>
Związki metali przejściowych
- > Powłoka walencyjna metali przejściowych
- > Efekt Jahna-Tellera
- > Teoria pola krystalicznego
- > Teoria pola ligandów
- > Widma elektronowe
- > Wiązania metal-metal
- > Własności magnetyczne
- > Trwałość związków koordynacyjnych
- > Związki z ligandami π–akceptorowymi
- > Arenowe związki koordynacyjne
- > Oddziaływania agostyczne
- > Wiązania chemiczne
- > Pojęcia chemii nieorganicznej
- > Mechanizmy reakcji
- > Oddziaływania międzycząsteczkowe
- > Elementy fizyki
- > Chemia organiczna
 Benzen
Benzen
W 1858 r. F. A. Kekulé zasugerował, że atomy węgla benzenu, a zwłaszcza naftalenu, są gęściej ułożone niż w większości związków organicznych („eine dichtere Aneinanderlagerung des Kohlenstoffes”). Wzór benzenu został po raz pierwszy zadowalająco zapisany przez Kekulé w 1865 roku. Podał także wskazówkę dotyczącą budowy tak zwanych „związków aromatycznych”, które zawierają zamknięte pierścienie atomów węgla, w przeciwieństwie do otwartych łańcuchów w tak zwanych „związkach tłuszczowych” lub „alifatycznych”. (Nazwy aromatyczne i alifatyczne pochodzą odpowiednio od Kekulé i Hofmanna). Geneza odkrycia została opisana przez Kekulé: podczas drzemki w swoim gabinecie w Gandawie zobaczył długie łańcuchy atomów węgla, jak węże skręcające się i zwijające, aż jeden „Chwycił własny ogon, a obraz wirował pogardliwie na moich oczach” (August Kekulé, Chemische Berichte, 1890, 23, 1306).
 August Kekulé, "Ueber einige Condensationsproducte des Aldehyds". Liebigs Ann. Chem., 1872, 162 (1): 77–124Sześć atomów węgla w pierścieniu benzenowym uznano za połączone na przemian pojedynczymi i podwójnymi wiązaniami, aby zachować czterowartościowość węgla. Kekulé początkowo używał ciekawych symboli, które zostały wyśmiane przez Kolbego, ale w 1865 roku użył kształtu sześciokąta dla benzenu bez wiązań, a w 1866 narysował szkic modelu przestrzennego z pojedynczymi i podwójnymi wiązaniami równoważny z nowoczesnym wzorem.
August Kekulé, "Ueber einige Condensationsproducte des Aldehyds". Liebigs Ann. Chem., 1872, 162 (1): 77–124Sześć atomów węgla w pierścieniu benzenowym uznano za połączone na przemian pojedynczymi i podwójnymi wiązaniami, aby zachować czterowartościowość węgla. Kekulé początkowo używał ciekawych symboli, które zostały wyśmiane przez Kolbego, ale w 1865 roku użył kształtu sześciokąta dla benzenu bez wiązań, a w 1866 narysował szkic modelu przestrzennego z pojedynczymi i podwójnymi wiązaniami równoważny z nowoczesnym wzorem.
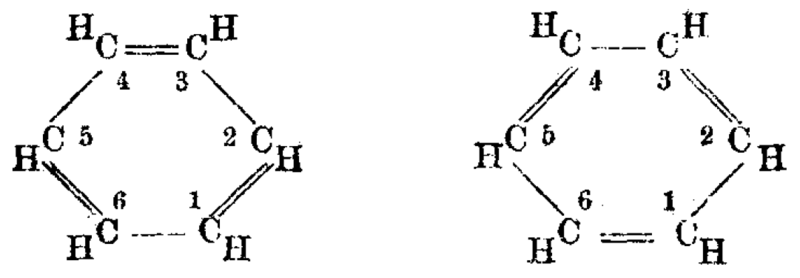
Istnienie wielokrotnych wiązań pomiędzy atomami węgla zostało uznane przez Kekulé w 1859 r., a w 1864 r. Crum Brown zapisał następujący wzór etylenu:

w którym wiązania podwójne zostały uwzględnione. Lothar Meyer w tym samym roku zaproponował, aby uznać etylen za zawierający dwa nienasycone powinowactwa, ponieważ cząsteczka łatwo łączy się z dwoma atomami chloru lub bromu w wyniku addycji, ale idea podwójnych wiązań Kekulé była preferowana, chociaż zapis wzoru tlenku węgla był utrudniony. Istnienie wiązań potrójnych w acetylenie zostało odkryte przez E. Erlenmeyera w 1862 roku.
Trudno przecenić rolę wzoru benzenu Kekulégo w chemii organicznej. Wyjaśniał on przypadki izomerii w pochodnych benzenu. Przed teorią Kekulé'a stwierdzono, że inne węglowodory aromatyczne są homologami benzenu, np. toluen został zsyntetyzowany przez W. R. Fittiga i B. Tollensa w 1864 r. z bromobenzenu i jodku metylu pod działaniem sodu, a zatem jest metylobenzenem. Ksylen, odkryty w surowym spirytusie drzewnym przez A. A. T. Cahoursa w 1849 r., również obecny w smole węglowej, jak wykazano jest dimetylobenzenem. W tym przypadku możliwe są trzy izomery, ponieważ dwie grupy metylowe znajdują się w pozycjach orto, meta lub para:

Określenie orientacji podstawników w takich przypadkach opracował Wilhelm Körner, asystent Kekulé, a później profesor w Mediolanie, w 1874 roku. Kekulé zwrócił uwagę, że izomeria może również powstać przez podstawienie, ponieważ to ostatnie występuje w pierścieniu lub w łańcuchu bocznym:

Chlor przyłączony do węgla w pierścieniu jest bardzo mocno związany i nie można go usunąć przez gotowanie z alkaliami, podobnie jak chloru w łańcuchu bocznym lub w związkach alifatycznych.
W 1866 r. E. Erlenmeyer zasugerował, że naftalen, odkryty przez A. Gardena i J. Kidda w smole węglowej, składa się z dwóch skondensowanych pierścieni benzenowych mających dwa wspólne atomy węgla. W wyniku utlenienia naftalenu kwas ftalowy został uzyskany przez A. Laurenta w 1836 r.; budowę naftalenu ustalił C. Gräbe, ponieważ bardzo łatwo tworzy bezwodnik w wyniku utraty wody, a zatem prawdopodobnie zawiera dwie grupy karboksylowe w dwóch sąsiadujących pozycjach:

Innym węglowodorem obecnym w smole węglowej jest antracen, odkryty w 1832 r. przez J-B. Dumasa i A. Laurenta. Jego wzór został wyjaśniony w 1868 r. przez C. Gräbe i C. Liebermanna, którzy wykazali, że składa się z trzech skondensowanych pierścieni benzenowych:

Wkrótce odkryto związki heterocykliczne, czyli zawierające w pierścieniu inne niż węgiel atomy, przykładowo pirydynę odkrył w 1869 roku W. Körner, i niezależnie od niego w 1871 roku J. Dewar.
Podsumowanie
Hermann Kolbe (1818–1884), profesor w Marburgu (1851) i Lipsku (1865), rozwinął poglądy Berzeliusa w okresie, gdy większość innych chemików je porzuciła. Zsyntetyzował kwas octowy (1844), uzyskał kwas metylosulfonowy (1845), badał elektrolizę soli kwasów tłuszczowych (1850), zsyntetyzował kwas salicylowy (1860), badał taurynę (1862), kwas malonowy (1864) i alifatyczne związki nitrowe (1872). Jego poglądy teoretyczne (1854–1865) zapowiadały współczesne wzory strukturalne i wartościowość oraz umożliwiły mu przewidywanie istnienia związków, które następnie zostały otrzymane, takich jak alkohole drugorzędowe i trzeciorzędowe.
Edward Frankland (1825–1899), profesor w Manchesterze (1851) i Londynie (1863), odkrył związki metaloorganiczne cynku (1849–64) rozszerzając badania nad kakodylem Bunsena; otrzymywał węglowodory z alkili cynku (1849), wysunął teorię wartościowości (1852–60) i opracował wzory strukturalne (1867). Uznał, że wartościowość pierwiastka może być różna. Z B. F. Duppą badał (1864 r.) reakcje i budowę estru acetooctowego (niezależnie odkrytego przez J. G. A. Geuthera w 1863 r.). Różne wartościowości pierwiastka w różnych związkach, np. Cl 1 w HCl i 7 w HClO4; S 2 w H2S, 4 w SO2 i 6 w H2SO4 zostały wyrażone przez Christiana Wilhelma Blomstranda (1826–1897), profesora w Lund (Chemie der Jetztzeit, Heidelberg, 1869), który również badał złożone związki amoniowe metali i (1869) przedstawił nazwę „związki diazoniowe” dla diazo-soli, co również niezależnie zaproponował A. Strecker (1871) i E. Erlenmeyer (1874). Teoretyczne poglądy Blomstranda oparte były na poglądach Berzeliusa, odpowiednio dostosowanych do teorii wartościowości.
August Kekulé (1829–1896), profesor w Gandawie (1858) i Bonn (od 1865), dodał do teorii typów „typ gazu błotnego” (1857) z jego podstawowym rodzajem gazem Ch. F. Gerhardta i uznał (jednocześnie z A. S. Couperem) czterowartościowość węgla (1857–8) oraz łączenie się atomów węgla. Zaproponował formułę sześciokąta dla benzenu (1865–6; 1872); prowadził badania w różnych gałęziach chemii organicznej (np. na związkach diazowych). Uważał, że wartościowość pierwiastka jest stała. Otrzymał acetylen w wyniku elektrolizy kwasu fumarowego (1864), zidentyfikował aldehyd krotonowy (1872) i odkrył trifenylometan (1872). Jego Lehrbuch der Organischen Chemie oder der Chemie der Kohlenstoffverbindungen (vol. I-III część 1 tomu IV jest niekompletna, Erlangen i Stuttgart, 1866-87) zawiera cenne wprowadzenie historyczne (vol. I , ss. 1-94).
Charles Adolphe Wurtz (18x7-1884), profesor w Paryżu, badał niższe tlenowe kwasy fosforu (1844-9), odkrył tlenochlorek fosforu, POCl3 (1846), powstawanie amin z izocyjanianów alkilowych (1848), syntezę węglowodorów z halogenków alkilu i sodu (1855), glikolu (1856), tlenku etylenu (1859), redukcję aldehydów do alkoholi za pomocą sodu (1862) i kondensację aldolową (1872). Uznanie jakim darzył poglądy Gerhardta znalazło oddźwięk w jego podręcznikach i miało istotny wpływ na rozwój teorii chemicznej.
Marcellin Berthelot (1827-1907), profesor w College de France w Paryżu, był jednym z najwybitniejszych chemików XIX wieku. Jego zainteresowania były wyjątkowo szerokie, a jego prace, z których wszystkie były oryginalne i miały fundamentalny charakter, można podzielić na cztery okresy: (I) na temat budowy i syntezy wieloatomowych alifatycznych alkoholi (w tym glicerolu) i kwasów organicznych ( 1850–60); (II) w sprawie syntezy węglowodorów, w tym syntezy acetylenu w łuku elektrycznym i jego polimeryzacji do benzenu, redukcji związków organicznych przez ogrzewanie w szczelnie zamkniętych probówkach z kwasem jodowodorowym oraz prace nad szybkością reakcji (z L. P. de Saint-Gilles) (1861–70); (III) badania termochemiczne, prace nad materiałami wybuchowymi (odkrycie „fali detonacyjnej”), ciepło właściwe gazów w wysokich temperaturach i synteza przy zastosowaniu wyładowań elektrycznych (1869–85); (IV) badania w zakresie historii chemii (1885-1907).