 Principles of Chemistry
Principles of Chemistry
- > Home
-
>
Historia chemii
- > Początki chemii
- > Rozwój alchemii
- > Jatrochemia
- > Badanie spalania i powietrza
- > Odkrycie i badanie gazów
- > Powstanie nowoczesnej chemii
- > Prawa chemiczne
- > Narodziny teorii atomowej
- > Elektrochemia
- > Berzelius, Hisinger, Faraday
- > Początki chemii organicznej
- > Substytucja
- > Wartościowość
- > Chemia fizyczna
- > Rozwój chemii nieorganicznej
- > Struktura atomu
-
>
Pierwiastki
- > Starożytność
- > Średniowiecze
- > Powietrze i woda
- > Analiza chemiczna
- > Halogeny
- > Elektrochemia
- > Metody spektroskopowe
- > Pierwiastki ziem rzadkich
- > Gazy szlachetne
- > Pierwiastki radioaktywne
- > Szeregi pierwiastków promieniotwórczych
- > Pierwiastki otrzymane sztucznie
- > Pierwiastki transuranowe
- > Podsumowanie
- > Układ okresowy
-
>
Mechanika falowa
- > Podstawy teoretyczne
- > Moment pędu
- > Równanie Schrodingera
- > Oscylator liniowy
- > Pole o symetrii sferycznej i pole kulombowskie
- > Spin
- > Identyczność cząstek
- > Oddziaływanie wymienne
- > Druga kwantyzacja
- > Poziomy energetyczne atomów
- > Układ okresowy
- > Atom w polu elektrycznym
- > Atom w polu magnetycznym
- > Cząsteczka dwuatomowa
- > Orto- i parawodór
- > Teoria relatywistyczna
- > Kwantowanie pola elektromagnetycznego
- > Fotony
- > Równanie Diraca
- > Cząstki i antycząstki
- > Atom i cząsteczka
-
>
Związki metali przejściowych
- > Powłoka walencyjna metali przejściowych
- > Efekt Jahna-Tellera
- > Teoria pola krystalicznego
- > Teoria pola ligandów
- > Widma elektronowe
- > Wiązania metal-metal
- > Własności magnetyczne
- > Trwałość związków koordynacyjnych
- > Związki z ligandami π–akceptorowymi
- > Arenowe związki koordynacyjne
- > Oddziaływania agostyczne
- > Wiązania chemiczne
- > Pojęcia chemii nieorganicznej
- > Mechanizmy reakcji
- > Oddziaływania międzycząsteczkowe
- > Elementy fizyki
- > Chemia organiczna
 Rozwój chemii organicznej
Rozwój chemii organicznej
Louis Pasteur urodził się w Dôle w 1822 r., Studiował w Arbois, następnie w Besançon, i wreszcie, od roku 1843, w paryskim Ècole normale,. Uczęszczał na wykłady zarówno A. J. Balarda, jak i J-B. Dumasa; pod kierunkiem G. Delafosse zajął się badaniem kryształów. W 1848 r. został profesorem fizyki w liceum w Dijon, w 1852 r. został profesorem chemii w Strasburgu, a w 1857 r. dyrektorem Ècole normale w Paryżu. Tam przeprowadził, w prywatnym laboratorium, badania nad fermentacją, które zapoczątkowały mikrobiologię, a w 1889 r. został założony Instytut Pasteura. Pracował tam aż do swojej śmierci w 1895 roku.
W latach 1815-35 J. B. Biot zaobserwował, że wiele naturalnie występujących związków organicznych, takich jak terpentyna, kamfora, cukry i kwas szczawiowy, wykazuje, w roztworach, właściwość skręcania płaszczyzny światła spolaryzowanego w jednym lub drugim kierunku. W 1844 r. A. Mitscherlich zauważył, że chociaż kwasy winowy i jego racemat są izomeryczne, to ten pierwszy jest optycznie czynny, podobnie jak jego sole, podczas gdy racemat jest nieaktywny. W 1848 r. Pasteur odkrył, że kryształy kwasu winowego charakteryzują się pewnym układem ścianek, których Mitscherlich nie zauważył, podobnie jak hemihedralne ściany obserwowane przez R. J. Haūya na optycznie czynnym krysztale kwarcu. Kryształy kwarcu można podzielić na dwie grupy, prawo- i lewoskrętne, zgodnie z położeniem ścian, przy czym te dwie formy wykazują relację obiektu i jego obrazu w lustrze. J. Herschel w 1821 r. zwrócił uwagę, że prawdopodobnie jest to związane z obserwacją Biota, że niektóre kryształy kwarcu obracają płaszczyznę spolaryzowanego światła w prawo, a niektóre w lewo. Jak widać, gdy Pasteur rozpoczął pracę nad kwasami winowymi związek między formą krystaliczną a aktywnością optyczną był dobrze ustalony. Jego ważnym odkryciem było to, że przez powolną krystalizację roztworu racematu sodowo-amonowego można było otrzymać kryształy optycznie czynne.
„Ostrożnie oddzieliłem kryształy, które były hemihedralne po prawej stronie od tych, które były hemihedralne po lewej stronie, i osobno zbadałem ich roztwory w aparacie polaryzacyjnym. Potem zobaczyłem z nie mniejszym zaskoczeniem niż przyjemnością, że hemihedralne kryształy po prawej stronie odchylają płaszczyznę polaryzacji w prawo, a te hemihedralne po lewej odchylają ją w lewo; a kiedy wziąłem taką samą wagę każdego z dwóch rodzajów kryształów, roztwór po ich zmieszaniu nie wykazywał aktywności wobec światła w wyniku neutralizacji dwóch równych i przeciwnych indywidualnych odchyleń.” Pasteur zauważa, że:„ Przez ponad trzydzieści lat Biot bezskutecznie usiłował nakłonić chemików do swojego przekonania, że badanie polaryzacji rotacyjnej stanowi jeden z najpewniejszych sposobów zdobycia wiedzy na temat budowy molekularnej substancji.” Dwa wolne kwasy winowe wydzielały ciepło po zmieszaniu, a z roztworu wykrystalizował ich związek, optycznie nieaktywny kwas racemiczny. Interpretacja wyników Pasteura pod względem składu chemicznego została podana niezależnie w 1874 r. przez J. van’t Hoffa i J. A. Le Bela.
Jacobus Henricus van't Hoff urodził się w Rotterdamie w 1852 roku. Kształcił się na Politechnice w Delft, na Uniwersytecie w Lejdzie, w Bonn pod kierunkiem F. A. Kekulé (którego uznał za niesympatycznego), a także pod kierunkiem Ch. A. Wurtza w École de Medecine w Paryżu, gdzie poznał Le Bela. W 1874 roku van't Hoff otrzymał doktorat w Utrechcie. W 1876 r. otrzymał stanowisko asystenta w Veterinary College w Utrechcie, gdzie napisał pierwszą część swojej Ansichten ūber die organische Chemie, oryginalnej książki, która według Jamesa Walkera „jest niemal nieczytelna” (J. Walker, Memorial Lecture, J. Chem. Soc., 1913, 1127). W 1878 roku został profesorem w Amsterdamie, gdzie spędził osiemnaście lat, ucząc chemii nieorganicznej i organicznej, krystalografii, mineralogii, geologii i paleontologii oraz prowadząc zajęcia praktyczne dla studentów medycyny. W tym okresie położył podwaliny pod współczesną chemię fizyczną.
W 1884 roku został opublikowany tekst Études de dynamique chimique van’ta Hoffa, w którym objaśniono ogólne zagadnienia dotyczące szybkości reakcji i zastosowania termodynamiki w chemii. Najważniejszą część stanowiło wyprowadzenie zależności między ciepłem reakcji a przesunięciem równowagi wskutek zmian temperatury, która jest nazywana izotermą van ’t Hoffa lub izotermą reakcji. Przy stałej objętości równowaga reakcji ulegnie zmianie w kierunku przeciwnym do temperatury (a narzuconym przez układ). W ten sposób obniżenie temperatury powoduje oddanie ciepła, natomiast jej podwyższenie jego absorpcję. Ostatnia część poświęcona jest badaniu powinowactwa mierzonego zmniejszeniem dostępnej energii, np. przez siły elektromotoryczne. Stosuje się równanie łączące ciepło reakcji ze zmianą stałej równowagi z temperaturą. Arrhenius powiedział o tej książce, że autorowi „udało się ze stosunkowo skąpym materiałem eksperymentalnym opracować imponujący i budzący grozę schemat dotyczący całego przedmiotu wpływu chemicznego i działania… przed przyszłymi badaniami otworzono ogromną perspektywę”.
W następnym roku wydał l’Equilibre chimique dans les systèmes gazeux ou dissous à l’état dilué (Równowaga chemiczna w gazach lub silnie rozcieńczonych roztworach), która dowodzi teorii rozcieńczonych roztworów. Pokazał, że w dostatecznie rozcieńczonych roztworach ciśnienie osmotyczne jest proporcjonalne do temperatury absolutnej, więc to ciśnienie może być przedstawione wzorem różniącym się od wzorów dla gazów jedynie współczynnikiem i. Ta praca została wydrukowana w Archives neerlandaises oraz w Transactions of the Swedish Academy. Nowe pomysły po raz pierwszy stały się szeroko znane, gdy zostały opublikowane wraz z fundamentalną rozprawą Arrheniusa w pierwszym tomie Zeitschrift fūr physikalische Chemie Ostwalda w 1887 r.
W 1896 van't Hoff przeprowadził się do Berlina jako profesor uniwersytetu z nominalnymi obowiązkami dydaktycznymi i laboratorium badawczym. Przeprowadził tam, wspólnie z W. Meyerhofferem i innymi, badania złóż soli w Stassfurcie, ale praca ta miała charakter rutynowy. Zmarł w 1911 r. „Bez wielkich osiągnięć matematycznych i eksperymentalnych”, pisze J. Walker, „bez uderzającego daru, jako nauczyciel, van't Hoff wpłynął i ukształtował obecną myśl, a nawet większość praktyki chemicznej na kolejne dekady.”
Stereochemia
We wrześniu 1874 roku ukazała się w Utrechcie broszura van’t Hoffa na temat wyników Pasteura (Voorstel tot uitbreiding der tegenwoordig in de scheikunde gebruikte structuur-formules in de ruimte); rozszerzone francuskie tłumaczenie (La chimie dans I’espace) pojawiło się w 1875 r. W listopadzie 1874 r. pojawia się w Bulletin de la Société Chimique tekst Le Bella. Sposoby rozumowania obu autorów różnią się nieco: Wydaje się, że na tok rozumowania van Hoffa miał większy wpływ Kekulé niż Pasteur, ale wyniki badań są praktycznie takie same. Argumenty Le Bella są bardziej abstrakcyjne, nie towarzyszą im rysunki i jest mniej zrozumiały, ale bardziej ogólny.
Według van't Hoffa: „W przypadku, gdy cztery powinowactwa atomu węgla są nasycone przez cztery różne jednoznaczne grupy, można uzyskać dwa i tylko dwa różne czworościany, z których jeden jest lustrzanym odbiciem drugiego …, dwa wzory strukturalne izomerów w przestrzeni.” Kekulé w 1867 roku opisał czworościenny model atomu węgla, z centralnym atomem w postaci kuli i czterema drutami skierowanymi do rogów czworościanu jako wartościowości. Ponadto, pisze van’t Hoff: „Każdy związek węgla, który w roztworze wykazuje skręcenie płaszczyzny polaryzacji, ma asymetryczny atom węgla”, to jest taki, w którym wszystkie cztery grupy związane z węglem są różne. W tym przypadku możliwe są dwa czworościany, zachowujące się jak obiekt i jego odbicie lustrzane. Przykładem tego rodzaju izomerii są optycznie czynne kwasy mlekowe badane przez J. Wislicenusa, który stosował idee van`t Hoffa.
Optycznie aktywne kwasy winowe zawierają dwa asymetryczne atomy węgla, a także możliwy jest trzeci izomer, w którym kompensują się dwa obroty wynikające z dwóch asymetrycznych atomów węgla, a cząsteczka jest nieaktywna jako całość. Ta postać, znana jako kwas mezowinowy, została otrzymana przez Pasteura; różni się od kwasu racemicznego, który jest połączeniem kwasów d– i l–winowego:

Prace J. Wislicenusa, E. Fischera, A. Baeyera, O. Wallacha i innych ustawiły teorię asymetrycznego atomu węgla na solidnym fundamencie.
Van’t Hoff w 1874 roku był również w stanie wyjaśnić izomerię kwasów fumarowego i maleinowego za pomocą izomerii geometrycznej. Czworościany otaczające dwa atomy węgla w cząsteczkach powinny być złączone wzdłuż krawędzi, reprezentując podwójne wiązanie, które uniemożliwiało obrót, a grupy H i COOH można następnie ułożyć w dwa modele, które się nie nakładają; nie są to izomery optyczne i różnią się właściwościami fizycznymi:
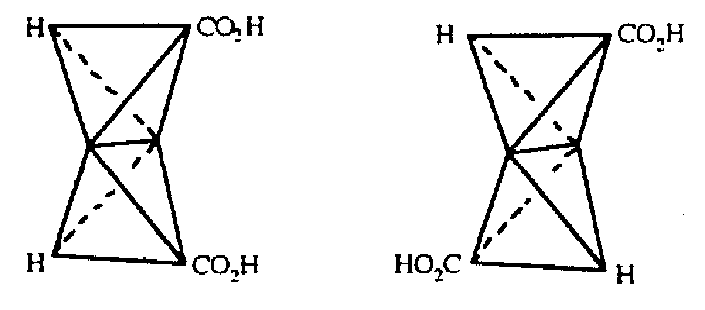 Kwas maleinowy i fumarowy van`t Hoffa
Kwas maleinowy i fumarowy van`t Hoffa
Udowodniono, że mogą istnieć optycznie aktywne związki, które nie zawierają asymetrycznego atomu węgla, ale mogą tworzyć dwie nie nakładające się konfiguracje cząsteczkowe: „aktywność optyczna nie jest spowodowana obecnością asymetrycznego atomu węgla, ale pochodzi z enancjomorficznej konfiguracji cząsteczkowej” (W. H. Perkin, W. J. Pope, O. Wallach, J. Chem. Soc., Trans., 1909, 95, 1789). Cząsteczki takich związków nie posiadają ani płaszczyzn ani środka symetrii i chociaż brak jest w nich asymetrycznego atomu węgla to wykazują aktywność optyczną. Późniejsze prace wykazały, że aktywność taką mogą przejawiać związki, w których cząsteczkach nie występują atomy węgla (P. Walden, Fünfzig Jahre stereochemischer Lehre und Forschung, Berichte der deutschen chemischen Gesellschaft, 1925, 58 (2), 237-265).
Syntetyczna chemia organiczna
Być może jedną z najbardziej uderzających cech chemii w drugiej połowie XIX wieku był niezwykle szybki rozwój syntetycznej chemii organicznej. Kiedy usunięto rozróżnienie między związkami nieorganicznymi i organicznymi, próby przygotowania w laboratorium związków, które gromadzą się w organizmach roślinnych i zwierzęcych, były podejmowane na coraz większą skalę, chociaż używane metody bardzo różnią się od metod stosowanych przez żywe komórki. Ponadto otrzymano wiele leków i barwników nie występujących w naturze. Trudno szczegółowo prześledzić rozwój tej gałęzi chemii, ale możemy przedstawić jej postępy, rozważając krótko pracę trzech wiodących chemików organicznych XIX wieku: Adolfa von Baeyera, Emila Fischera i Victora Meyera.
Adolf Baeyer urodził się w 1835 roku w Berlinie, a w 1853 roku udał się do Heidelbergu, aby studiować u R. Bunsena. Pracował również z Kekulé, w 1858 r. przedstawił pracę magisterską na temat związków kakodylowych. W tym samym roku podążył za Kekulé do Gandawy gdzie pracował nad pochodnymi kwasu moczowego. W 1860 wrócił do Berlina i przez dwadzieścia lat nauczał w szkole technicznej, gdzie kontynuował pracę nad kwasem moczowym. W 1872 r. został profesorem na uniwersytecie w Marburgu, gdzie dołączył do niego Emil Fischer. Prowadzili prace nad kondensacją węglowodorów aromatycznych i fenoli z aldehydami. W 1875 r. wyjechał do Monachium obejmując stanowisko po Liebigu. Zmarł w 1917 roku.
 W 1870 r. Baeyer i A. Emmerling przeprowadzili pierwszą syntezę indygo, niebieskiego barwnika, którego wzór empiryczny, C16H5NO2, został określony przez J-B. Dumasa w 1840 r. Syntezę przeprowadzono przez ogrzewanie chlorku izatyny z fosforem i kwasem jodowodorowym. W latach 1878–1884 Baeyer przeprowadził badania indygo i jego pochodnych.
W 1870 r. Baeyer i A. Emmerling przeprowadzili pierwszą syntezę indygo, niebieskiego barwnika, którego wzór empiryczny, C16H5NO2, został określony przez J-B. Dumasa w 1840 r. Syntezę przeprowadzono przez ogrzewanie chlorku izatyny z fosforem i kwasem jodowodorowym. W latach 1878–1884 Baeyer przeprowadził badania indygo i jego pochodnych.
Zniechęcony sposobem działania niemieckich firm farbiarskich, z którymi związany był Baeyer, wzbudziły w nim niechęć do tego tematu i zwrócił uwagę na badanie pochodnych acetylenu. Opracował metody syntezy szeregu związków, na przykład kwasu tetraacetylenodikarboksylowego, niektóre z nich są wysoce wybuchowe. Założył, że niestabilny charakter takich związków jest spowodowany naprężeniem wynikającym z obecności w cząsteczce szeregu wiązań, tworząc tzw. „teorię odkształceń Baeyera”. Baeyer wykazał, że benzen można zredukować przez wprowadzenie sześciu atomów wodoru do heksahydrobenzenu substancji nie posiadającej żadnych właściwości związków aromatycznych, a także pracował nad terpenami, olejkami eterycznymi i kamforą.
 Badania Baeyera nad pochodnymi indygo doprowadziły go w 1882 r. do wniosku, że ta sama substancja może zachowywać się w stosunku do różnych odczynników, tak jakby miała dwa różne wzory strukturalne. Zjawisko to nazwano tautomerią. Zostało ono początkowo wyjaśnione oscylacją wiązań w cząsteczce (J. von Laar, 1885), ale później zasugerowano, że substancja tautomeryczna jest mieszaniną dwóch form pozostających w równowadze, które łatwo przekształcają się w siebie (izomeria dynamiczna). Wykazano, że tak jest w przypadku estru acetylooctowego poprzez izolację tych dwóch form przez L. Knorra i Kurta Meyera w 1911 i 1920:
Badania Baeyera nad pochodnymi indygo doprowadziły go w 1882 r. do wniosku, że ta sama substancja może zachowywać się w stosunku do różnych odczynników, tak jakby miała dwa różne wzory strukturalne. Zjawisko to nazwano tautomerią. Zostało ono początkowo wyjaśnione oscylacją wiązań w cząsteczce (J. von Laar, 1885), ale później zasugerowano, że substancja tautomeryczna jest mieszaniną dwóch form pozostających w równowadze, które łatwo przekształcają się w siebie (izomeria dynamiczna). Wykazano, że tak jest w przypadku estru acetylooctowego poprzez izolację tych dwóch form przez L. Knorra i Kurta Meyera w 1911 i 1920:
Emil Fischer urodził się w 1852 r. w Euskirchen, niedaleko Bonn, i w 1871 roku został uczniem Kekulé. Studia ukończył u Baeyera w Strasburgu w 1874 r., był profesorem w Erlangen w 1882 r. i Wūrzburg w 1885 r. W 1892 r. zajął stanowisko piastowane wcześniej przez A. W. Hofmanna w Berlinie, gdzie pozostał do śmierci w 1919 r. Badania Fischera stanowią przykład wysokiej specjalizacji w syntetycznej chemii organicznej, która nabierała rozpędu w drugiej połowie XIX wieku.
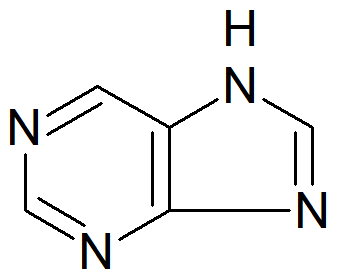 purynaW początkowym okresie prac Fischera było odkrycie, w 1875 r. fenylohydrazyny, C6H5-NH-NH2, która w rękach Fischera stała się odczynnikiem ogólnym dla grupy karbonylowej. W 1884 r. odkrył, że cukry reagowały w charakterystyczny sposób z fenylohydrazyną i wywnioskowano obecność grup karbonylowych w ich cząsteczkach. W 1887 Fischer i J. Tafel odkryli, że z akroleiny H2C=CH-CHO można uzyskać dwa syntetyczne cukry, z których jeden jest identyczny z naturalną fruktozą. Dzięki zastosowaniu pomysłowych reakcji i metod stosowanych przez Pasteura otrzymał optycznie czynne cukry dekstrozę, fruktozę i mannozę. W 1891 roku zbadał konfigurację cząsteczek cukru i opracował ich wzory strukturalne. Od badania cukrów Fischer przeszedł do innej grupy naturalnych substancji, pochodnych puryn, do których należą kofeina oraz kwas moczowy. Wcześniej J. Liebig i F. Wôhler badali niektóre pochodne kwasu moczowego. Fischer wykazał, że ta grupa substancji wywodzi się z organicznej zasady, puryny. Około 130 pochodnych puryn zostało zbadanych przez Fischera i jego studentów przed 1900 rokiem.
purynaW początkowym okresie prac Fischera było odkrycie, w 1875 r. fenylohydrazyny, C6H5-NH-NH2, która w rękach Fischera stała się odczynnikiem ogólnym dla grupy karbonylowej. W 1884 r. odkrył, że cukry reagowały w charakterystyczny sposób z fenylohydrazyną i wywnioskowano obecność grup karbonylowych w ich cząsteczkach. W 1887 Fischer i J. Tafel odkryli, że z akroleiny H2C=CH-CHO można uzyskać dwa syntetyczne cukry, z których jeden jest identyczny z naturalną fruktozą. Dzięki zastosowaniu pomysłowych reakcji i metod stosowanych przez Pasteura otrzymał optycznie czynne cukry dekstrozę, fruktozę i mannozę. W 1891 roku zbadał konfigurację cząsteczek cukru i opracował ich wzory strukturalne. Od badania cukrów Fischer przeszedł do innej grupy naturalnych substancji, pochodnych puryn, do których należą kofeina oraz kwas moczowy. Wcześniej J. Liebig i F. Wôhler badali niektóre pochodne kwasu moczowego. Fischer wykazał, że ta grupa substancji wywodzi się z organicznej zasady, puryny. Około 130 pochodnych puryn zostało zbadanych przez Fischera i jego studentów przed 1900 rokiem.
W 1899 r. rozpoczęły się jego badania nad aminokwasami. Najprostszym aminokwasem jest kwas aminooctowy, glicyna: H2N-CH2-COOH. W wyniku kondensacji powstaje glicyloglicyna: H2N-CH2-CO-NH-CH2-COOH. Fischer stopniowo rozszerzał cząsteczki kondensatów aż w 1907 roku doszedł do:
H2N-CH(C4H9)-CO(NH-CH2-CO)3-NH-CH(C4H9)-CO-(NH-CH2-CO)3-NH-CH(C4H9)-CO(NH-CH2-O)8-NH-CH2-COOH.
Skomplikowanego organicznego aminokwasu, którego cząsteczka przypomina jedną z naturalnych albumin. Ten polipetyd ma 816 naturalnych izomerów.
Viktor (lub Victor ponieważ używał obu form imienia) Meyer urodził się w 1848 r. w Berlinie, studiował u Bunsena w Heidelbergu od 1865 r. i został jego asystentem; w 1868 roku wyjechał do Berlina, aby współpracować z Baeyerem nad chemią organiczną. Po krótkim pobycie w Wūrtemburgu został profesorem na Politechnice w Zurychu w 1872 r. W 1885 r. przeniósł się do Getyngi, a w 1889 r. do Heidelbergu. Zmarł w 1897 r.
W 1874 roku badał alifatyczne związki nitrowe, stwierdzając, że nitroetan zachowuje się jak kwas w stosunku do wodorotlenku sodowego, co sugerowało występowanie tego typu związków w formach tautomerycznych:
C2H5-NO2 ↔ C2H5-NO(OH)
W 1877 r. opisano znaną metodę określania masy cząsteczkowej na podstawie gęstości par, która została zmodyfikowana w późniejszych pracach, tak aby można było przeprowadzić oznaczenia w wysokich temperaturach. Wykazano, że w wysokich temperaturach cząsteczki bromu i jodu ulegają dysocjacji na atomy. W 1882 r. zbadano działanie hydroksyloaminy na aldehydy i ketony i odkryto ważną grupę związków, oksymów, w których grupa karbonylowa aldehydu lub ketonu jest skondensowana z hydroksyloaminą.
 W 1882 r. w trakcie wykładu Victor Meyer odkrył, że próbka benzenu nie wywołała reakcji indofenolowej opisanej przez Baeyera, czyli powstawania niebieskiego zabarwienia w kontakcie ze stężonym kwasem siarkowym(VI) i izatyną. Stwierdził, że benzen przygotowany do pokazu na wykładzie został przygotowany z kwasu benzoesowego i był bardzo czysty; zwykły benzen ze smoły węglowej, który dawał taką reakcję zawierał nową substancję, tiofen, związek siarki zawierający pięcioczłonowy pierścień, który został odkryty w 1883 r. przez Victora Meyera. Jest analogiczny do furanu (którego pochodna, furfurol, został odkryty przez J. W. Döbereinera w 1831 r. i G. Fownesa w 1845 r.) i pirolu (odkryty, ale nie analizowany przez F. F. Runge, 1834 r .; wzór opracowany przez A. Baeyera, 1866).
W 1882 r. w trakcie wykładu Victor Meyer odkrył, że próbka benzenu nie wywołała reakcji indofenolowej opisanej przez Baeyera, czyli powstawania niebieskiego zabarwienia w kontakcie ze stężonym kwasem siarkowym(VI) i izatyną. Stwierdził, że benzen przygotowany do pokazu na wykładzie został przygotowany z kwasu benzoesowego i był bardzo czysty; zwykły benzen ze smoły węglowej, który dawał taką reakcję zawierał nową substancję, tiofen, związek siarki zawierający pięcioczłonowy pierścień, który został odkryty w 1883 r. przez Victora Meyera. Jest analogiczny do furanu (którego pochodna, furfurol, został odkryty przez J. W. Döbereinera w 1831 r. i G. Fownesa w 1845 r.) i pirolu (odkryty, ale nie analizowany przez F. F. Runge, 1834 r .; wzór opracowany przez A. Baeyera, 1866).
W 1891 r. Victor Meyer przeprowadził badania temperatur zapłonu wybuchowych mieszanin gazowych ujawniając wyraźny wpływ ścian pojemnika zawierającego gaz. W 1893 r. zbadano dysocjację kwasu jodowodorowego i wykazano, że jest to reakcja odwracalna. W latach 1892-94 Meyer i jego uczniowie badali organiczne związki jodu. W latach 1894–1897 prowadził badania nad zawadą steryczną. Podczas gdy kwas benzoesowy i większość jego produktów podstawienia, z łatwością tworzą estry z alkoholem w obecności chlorowodorem, to trójpodstawione kwasy benzoesowe takim reakcją nie podlegają, chyba że grupa karboksylowa znajduje się poza pierścieniem benzenowym w łańcuchu alifatycznym,
Uważano, że podstawniki w pozycji otro znajdują się tak blisko grupy karboksylowej, że wywierają pewien efekt, czego nie obserwuje się, gdy ta grupa znajduje się na końcu łańcucha alifatycznego. Obecnie wiadomo, że to wyjaśnienie jest prawdziwe tylko w niektórych przypadkach, a „efekt orto” jest związany z właściwościami elektrochemicznymi („polarnymi”) grup podstawników, co z pewnością zadowoliłoby Berzeliusa.
Podsumowanie
Louis Pasteur (1822–95), profesor w Strasburgu i Pans, a od 1889 dyrektor Instytutu Pasteura, badał aktywność optyczną, obserwując hemihedralne płaszczyzny na kryształach kwasu winowego i winianów, które nie występowały w przypadku racematach, i otrzymując związek nieaktywny optycznie, racemat sodowo-amonowy przez krystalizację (1848-50). Rozdzielił także substancje racemiczne lub optycznie nieaktywne przez frakcjonowaną krystalizację z optycznie czynnym kwasem lub zasadą (1853). Odkrył kwas L-winowy i mezowinowy. Pasteur dostarczył eksperymentalne dowody na witalistyczną teorię fermentacji (1857), a później przeprowadził fundamentalne badania w bakteriologii, obalając teorię samorództwa.
Związek aktywności optycznej z obecnością w cząsteczce asymetrycznego atomu węgla określili niezależnie od siebie w 1874 r. van't Hoff i Le Bel. Badania aktywności optycznej zostały przeprowadzone przez profesora z Berlina Hansa Landolta (1831–1901), który zbadał także organiczne związki arsenu i antymonu (1853 r.) i model zależności refrakcji substancji zaproponowany w 1858 r. przez Johna Hall Gladstone’a (1827-1902) i J. Dale’a. Refrakcje cząsteczkowe z teoretycznego punktu widzenia zaproponowanego niezależnie w 1880 r. przez L. Lorenza i H. Lorentza, badał od 1880 r. J. W. Brūhl (1850–1911), ze szczególnym uwzględnieniem wpływu struktury związku.
Emil Erlenmeyer, (1825–1909), profesor Monachijskiej Szkoły Politechnicznej, zaproponował teorię wartościowości (1863) i sposób zapisywania struktur związków (1867), odkrył kwas izomasłowy (1865), budowę czasteczki naftalenu (1866) oraz kwasów hydroksykarboksylowych i mlekowych (1867), wyjaśnił strukturę laktonów (1880), zsyntetyzował tyrozynę (1883).
Alexander Michaiłowicz Butlerow (1828–86), profesor w Petersburgu, otrzymał syntetyczne heksozy („metylenitan”) (1861) i trzeciorzędowe alkohole z alkili cynku i chlorków kwasowych (1864); badał izomeryczne dibutyleny, stwierdzając istnienie „izomerii dynamicznej” (1877).
Johann Peter Griess (1829–88) odkrył aromatyczne związki diazowe (1858; opublikowane w 1860). Alifatyczne pochodne diazowe zostały odkryte w 1894 r. przez Hansa von Pechmanna (1850–1904), profesora w Tybindze, w wyniku działania alkaliów na nitrozoaminy.
Carl Schorlemmer (1834-1892), asystent (1859), a następnie profesor (1874) chemii organicznej w Manchesterze, pracował nad węglowodorami parafinowymi (1861 i nast.), wykazał, że rzekomo wolny metyl, CH3 i wodorek etylu, C2H5·H, uważane za izomery, były tym samym związkiem o wzorze C2H6. Odkrył ogólną metodę konwersji alkoholi drugorzędowych do pierwszorzędowych (1866), badał temperatury wrzenia parafin (1872) oraz konstytucję auryny (1871) i suberonu (1874). Współpracował z H. Roscoe przy opracowaniu traktatu o chemii (1877 i nast.), w którym część poświęcona chemii organicznej nie została dokończona w wydaniu angielskim, ale została uzupełniona przez Brūhla w tłumaczeniu na język niemiecki.
Rudolf Fittig (1835–1910), profesor w Tybindze (1869) i Strasburgu (1876), odkrył reakcję sprzęgania pinakolu (1859) i difenylu (1862), zsyntetyzował węglowodory aromatyczne poprzez działanie sodu na mieszaninę halogenków alkilu i arylu („Reakcja Fittiga”) (z B. Tollensem, 1864), zsyntetyzował mezytylen (1867), odkrył kwas izoftalowy (1867), badał sole złożone (np. K4Mn(CN)6 i K3Mn(CN)6) (1868), badał piperynę (1869), odkrył fenantren (1872), zaproponował wzór diketonowej formy chinonu (1873-6), badał nienasycone kwasy karboksylowe (1877- 1904), odkrył kumaron (1883), zsyntetyzował a-naftol (1885), badał estry ketonowe (1887), odkrył diacetyl (1887) i wykazał związek pomiędzy g-hydroksykwasami i laktonami (1881- 1904).
William Henry Perkin (1838-1907), otrzymał pierwszy barwnik „anilinowy” (1856), glikokol (Perkin i B. F. Duppa, 1858), kwas winowy (Perkin i Duppa, 1861), kumarynę (1868) i kwas cynamonowy (1877: „reakcja Perkina”), badał skład saligeniny (1868) i związek między magnetyzmem cząsteczek a składem chemicznym (1884–1907).
Johann Wislicenus (1835–1902), profesor w Wūrzburgu i Lipsku, badał kondensację aldehydową (1857–8) i kwasy mlekowe (1863–75). Przyjął i rozwinął stereochemiczne teorie van't Hoffa (od 1875 r.). Od 1874 r. Wislicenus i jego uczniowie (M. Conrad, L. Limpach) badali zastosowanie estru acetylooctowego (odkrytego przez J. G. A. Geuthera w 1863 r., A niezależnie przez E. Franklanda i B. F. Duppy w 1865 r.) w syntezach organicznych, np. syntezując kwas glutarowy (1878), keton metylo-b-butylowy (1883) itp. Conrad i Limpach (1874-7) opracowali szczegóły metody syntezy w zależności od interakcji pochodnej sodowej estru acetlooctowego i jodku alkilu. Wislicenus odkrył eter winylowy (1878) i kwas winylooctowy (1899). Ważne jest jego odkrycie prostej syntezy kwasu hydratowego (1892) i jego prace na temat izomerii geometrycznej związków nienasyconych (1887–9).
Adolf Baeyer (1835–1917), profesor w Berlinie i Monachium, badał pochodne puryn (1861–70), odkrył indol oraz budowę i syntezę indygo (1866–85); wysunął teorię odkształceń pierścieni węglowych (1885), zbadał produkty redukcji benzenu i jego pochodnych (1888-93), badał terpeny (1893-99). Chemię terpenów badali także Albin Haller (1849–1925) w Paryżu, Otto Wallach (1847–1931) w Getyndze, William Henry Perkin i Gustav Komppa (ur. 1867) w Helsingfors.
Wilhelm Körner (1839–1925), profesor z Mediolanu, zaproponował wzór pirydyny (1869), opracował metodę określania orientacji produktów podstawienia benzenu (1874) i zsyntetyzował asparaginę (z A. Menozzi, 1887).
Albert Ladenburg (1842–1911), profesor we Wrocławiu, zaproponował budowę pryzmatu dla benzenu (1869), badał alifatyczne (1867–72) i aromatyczne (1873–4) związki krzemu (częściowo w połączeniu z Charlesem Friedelem), zsyntetyzował optycznie czynną koniinę (1886) i pracował nad budową innych alkaloidów (od 1879).
Jacob Volhard (1834–1910), profesor w Halle, zsyntetyzował sarkozynę (1862) i kreatynę (1868), opracował argentometryczne miareczkowanie tiocyjanianem srebra (1874), zsyntetyzował tiofen (1885).
Carl Gräbe (1841-1927), profesor w Genewie, wykazał, że alizaryna ulega redukcji do antracenu podczas destylacji z pyłem cynkowym (z C. Liebermannem, 1868), opracował metodę syntezy alizaryny z antrachinonu (z C. Liebermannem, 1869), określił skład antracenu (z Liebermannem, 1869), odkrył akrydynę (z H. Caro, 1870), wyizolował i zsyntetyzował karbazol (z C. A. Glaserem, 1872), zsyntetyzowane pochodne chinoliny (1878) i acenafteny (1893). Badał także barwniki.
Carl Liebermann (1842–1914), profesor w Berlinie, badał działanie kwasu azotawego(V) na fenole i drugorzędowe aminy („reakcja Liebermanna”) (1874), opracował skład antrachinonu i alizaryny (z C. Gräbe, 1868–82), antracenu i fenantren (z C. Gräbe, 1869–70), kwerceytyny i ramnetyny (1879).
Viktor Meyer (1848-97), profesor w Zurychu i Heidelbergu, odkrył alifatyczne nitro-związki (1872), związki izonitrosowe i nitryle (1S75-82), tiofen (1882), oksymy i ich izomerię (1883-90), organiczne związki tlenowe jodu (1892-7) oraz występowanie zawady przestrzennej w związkach organicznych (1894-7). W chemii fizycznej opracował nową metodę wyznaczania gęstości par (1878–80), badał szybkości reakcji i równowagę oraz przeprowadzał badania w wysokich temperaturach.
Emil Fischer (1852–19 x 9), profesor w Berlinie, zbadał skład rozaniliny (1878), odkrył fenylohydrazynę (1875) i zastosował ją jako odczynnik w szeroko zakrojonych badaniach dotyczących budowy, syntezy i konfiguracji cukrów (1884-1900); zbadał i zsyntetyzował kilka zasad purynowych (1882–1901); dokonał syntezy polipeptydów (1900-06); badał inwersję Waldena (1908-12) i pracował nad budową i syntezą garbników (1912-19). Chemię polipeptydów i białek badał Emil Abderhalden (ur. 1877).
Theodor Curtius (1857-1928), profesor w Heidelbergu, odkrył ester diazooctowy (1883), hydrazynę (1887), kwas hydrazowy i jego pochodne (1890), pochodne pirazoliny (1891), benzaldazynę i aldazyny (1900) oraz inne pochodne tetrazyny (1906). Pracował nad estrami glikolowymi (1883) i polipeptydami (1904).
Erast Beckmann (1853–1923), profesor w Erlangen i Lipsku, udoskonalił metody oznaczania temperatury krzepnięcia (1888) i temperatury wrzenia (1889) wykorzystywane do określania masy cząsteczkowej w roztworach konstruując odpowiednie urządzenie; w chemii organicznej odkrył przegrupowanie oksymów (1886, „przegrupowanie Beckmanna”), opracował metodę otrzymywania tymolu z mentolu (1896) i zbadał możliwe techniczne zastosowania furfurolu (1919); w chemii nieorganicznej badał wyższe chlorki siarki (1909 i nast.).
Ludwig Claisen (1851–1930), profesor w Aix-la-Chapelle i Kilonii, opracował metody syntez aromatycznych ketoestrów (1881), benzylidenoaceton (1881) i ester benzoilooctowy (1887). Wyjaśnił mechanizm syntezy estru acetylooctowego jako wynik pośredniego tworzenia orto-związku (1887–8, 1897); opracował syntezy b-diketonów przez kondensację ketonów i estrów kwasowych w obecności sodu, etanolanu sodu lub amidku sodu (1887, kondensacja Claisena); otrzymał pirazol (wcześniej L. Knorr w 1885, Emil Fischer 1885) i pochodne dipirazolu z 1,3-diketonów i oksalilodiacetonu z fenylohydrazyną (1894); badał przypadki izomerii i tautomerii form keto– i enolowych, którą wykazał na przykładzie acetyldibenzoilometanu (1892).
Eugen Bamberger (1857–1932), profesor w Zurychu, badał pochodne guanidyny (1880), odkrył piren (1887), wprowadził stosowanie sodu i alkoholu amylowego jako środka redukującego (1887 ), badał produkty redukcji naftyloamin (1888), kwasu cyjanurowego (1890), cyjanamin (1892), redukcję nitrobenzenu do nitrozobenzenu i fenylohydroksyloaminy (1894), benzamidu (1899), tlenku dimetyloaniliny (1899) oraz izomerię związków nitrozowych (1903). Zaangażował się w A. Hantzschem w długą dyskusję (1894–1900) dotyczącą budowy związków diazowych.
Arthur Hantzsch (1857-1935), profesor w Lipsku, pracował nad syntezą pirydyny z estru acetylooctowego, aldehydu i amoniaku (1882), kumaronu (1886), tiazolu (1889), stereochemii związków zawierających azot, oksymów (z A. Wernerem, 1890) i związków diazowych (1894), Wyizolował kwas diazotowy(I) (1896), badał zachowanie tautomeryczne fenylonitrometanu i nitrofenoli jako pseudo-kwasów (1899; 1905), strukturę kwasu cyjanurowego i cyklicznych amidów (1905 i nast.), zastosował metody fizykochemiczne (np. przewodnictwo elektryczne) w chemii organicznej oraz zaawansowane teorie wskaźników (1907) i budowy kwasów (1917-25).
Ludwig Knorr (1859–1921), profesor w Jenie, badał pirazolon i izopyrazolon oraz ich pochodne (1883–1911), odkrywając ważny lek antypirynę (fenylodimetylopirazolon, 1887). Jego praca nad związkami wykazującymi tautomerię, takimi jak ester diacetylobursztynowy (1896 1), ester acetylooctowy (1904) i acetyloaceton (z H. Fischerem, 1911), skłoniła go do rozważenia substancji tautomerycznej jako mieszaniny dwóch form w stanie równowagi na co był w stanie dostarczyć dowody eksperymentalne. Opracował kolorymetryczną metodę określania proporcji formy enolowej w jej tautomerycznej mieszaninie z formą ketonową (z H. Schubert, 1911). Opracował metodę otrzymywania acetonyloacetonu (1900), odkrył eter aminoetylowy (z G. Meyerem, 1905), pracował nad pochodnymi piperazyny i alkaloidami (1904).
William Henry Perkin (1860–1929), profesor w Heriot Watt College Edynburg (1887–92), Manchesterze (1892–1913) i Oksfordzie (1913–29), dokonał syntez pierścieni polimetylenowych (1883–94), octanu benzoilu etylu i pochodnych ( 1884-6), antrachinonu przez ogrzewanie kwasu orto-benzoilooctowego z kwasem siarkowym (1891), indenu i hydrindenu i pochodnych (18941), kwasów di- i tri-metyloglutarowych z pochodnymi (1895), kamfory i jej pochodnych (1897. synteza kwasu kamforonowego z J. F Thorpe, 1897), alkaloidów (1890–1929: berberyna, narcyna, kotarnina, kryptopina, protopina, strychnina); terpenów (1904–21; synteza terpineolu, 1904), hematoksyliny (1901–28), harminy i harmaliny (1912–27) oraz pochodnych izochinoliny (1925–6). Jego praca nad pierścieniowymi polietylenami doprowadziła do teorii odkształceń Baeyera (1885).
Johannes Thiele (1865–1918), profesor w Monachium i Strasburgu, odkrył semikarbazyd (1894), zbadał pochodne tetrazolu (1895) i nitramid (1895), odkrył pochodne fulwenu (1900), zbadał pochodne guanidyny (1892) i nienasyconych laktonów (1899–1902); wysunął (1899) teorię „częściowych wartościowości” w celu wyjaśnienia reakcji addycji do podwójnych wiązań i budowy benzenu.
Victor Grignard (1871–1935), profesor w Nancy i Lionie, opracował tak zwaną reakcję Grignarda (1900) - częściowo odkrytą przez jego nauczyciela P. A. Barbiera - która zastąpiła użycie alkilków metali w reakcjach syntetycznych przez związki magnezoorganiczne (MgRX) w roztworach eterowych.
Richard Willstätter (1872–1942), profesor w Monachium i Berlinie, badał alkaloidy i ich pochodne (kwas tropowy, tropina, atropina, ekgonina i kokaina) (1896–1903), opracował syntezę betainy (1902), lecytyny (1904), orto-chinonów, chinonoimin i pironów (1904); badał barwniki roślinne: chlorofil (1906), antocyjanina i barwniki krwi (1913), asymilację dwutlenku węgla przez rośliny (1917) i enzymy (1921).
Paul Sabatier (1854–1941) uzyskał czysty dwusiarczek wodoru (1886) i wprowadził metodę katalitycznego uwodornienia (od 1897 r.).
Henry Edward Armstrong (1848–1937), uczeń Hofmanna i Franklanda w Londynie i Kolbego w Lipsku (1867), profesor w Instytucie Londyńskim, Finsbury Circus (1871) oraz City and Guilds Institute (1879–1911); badania nad pochodnymi naftalenu (1881–1900), terpenami i kamforą (1878–1902) oraz chinonoidową teorią barwników (1888, 1892); pisał o chemii nieorganicznej, chemii organicznej i nauczaniu przedmiotów ścisłych. Był zapalonym krytykiem teorii dysocjacji elektrolitycznej.
William Jackson Pope (1870–1939), profesor w Manchester School of Technology (1901) i w Cambridge (1908), pracował głównie w dziedzinie stereochemii, szczególnie związków optycznie czynnych, w tym pierwiastków innych niż węgiel; wprowadził kwasy kamforosulfonowe do rozdzielania optycznie czynnych zasad i hydroksyhydrindaminę (z J. Read) do rozdzielaniu kwasów; z C. S. Gibsonem otrzymał siarczek dichlorodietylu („gaz musztardowy”) przez działanie etylenu na chlorek siarki (1920).
Gilbert Thomas Morgan (1870–1940), asystent w Royal College of Science, profesor w Dublinie (1912) i Birmingham (1919) oraz kierownik Laboratorium Badań Chemicznych, Teddington (1927); badania barwników; związków organicznych arsenu, antymonu, selenu i telluru; związków koordynacyjnych; procesów uwodornienia katalitycznego; produktów kondensacji fenolowo-formaldehydowej.
Arthur Lapworth (1872-I941) kierownik działu chemii w Goldsmiths' Institute, Londyn (1900), wykładowca chemii nieorganicznej i fizycznej (1909), profesor chemii organicznej (19I3) i chemii fizycznej i nieorganicznej (1922) w Manchesterze; pionier chemii organicznej opartej na elektronowej teorii wartościowości; badanie procesów powstawania cyjanohydryny (1907); mechanizmu estryfikacji (1908 f.); enolowo-ketonowy mechanizm bromowania acetonu (19I3); badanie podstawowych właściwości wody i alkoholu oraz próby stworzenia ogólnej teorii kwasów i zasad (1908), opracowanej później przez Lowry'ego i Brønsteda.
Jocelyn Field Thorpe (1872–1940) początkowo studiował inżynierię, a później chemię w Londynie i Heidelbergu; wykładowca w Manchesterze (1897) i (1913) profesor w Imperial College w Londynie; badania nad kamforą i terpenami (Perkin i Thorpe, synteza kwasu kamforonowego, 1897 i kwasu kamforowego, 1903, niezależnie od G. Komppy, 1903); związki iminowe i pochodne hydrindenu (1904), kwasy glutakonowe (1923); tautomeria i związki bicykliczne (1911).