 Principles of Chemistry
Principles of Chemistry
- > Home
-
>
Historia chemii
- > Początki chemii
- > Rozwój alchemii
- > Jatrochemia
- > Badanie spalania i powietrza
- > Odkrycie i badanie gazów
- > Powstanie nowoczesnej chemii
- > Prawa chemiczne
- > Narodziny teorii atomowej
- > Elektrochemia
- > Berzelius, Hisinger, Faraday
- > Początki chemii organicznej
- > Substytucja
- > Wartościowość
- > Chemia fizyczna
- > Rozwój chemii nieorganicznej
- > Struktura atomu
-
>
Pierwiastki
- > Starożytność
- > Średniowiecze
- > Powietrze i woda
- > Analiza chemiczna
- > Halogeny
- > Elektrochemia
- > Metody spektroskopowe
- > Pierwiastki ziem rzadkich
- > Gazy szlachetne
- > Pierwiastki radioaktywne
- > Szeregi pierwiastków promieniotwórczych
- > Pierwiastki otrzymane sztucznie
- > Pierwiastki transuranowe
- > Podsumowanie
- > Układ okresowy
-
>
Mechanika falowa
- > Podstawy teoretyczne
- > Moment pędu
- > Równanie Schrodingera
- > Oscylator liniowy
- > Pole o symetrii sferycznej i pole kulombowskie
- > Spin
- > Identyczność cząstek
- > Oddziaływanie wymienne
- > Druga kwantyzacja
- > Poziomy energetyczne atomów
- > Układ okresowy
- > Atom w polu elektrycznym
- > Atom w polu magnetycznym
- > Cząsteczka dwuatomowa
- > Orto- i parawodór
- > Teoria relatywistyczna
- > Kwantowanie pola elektromagnetycznego
- > Fotony
- > Równanie Diraca
- > Cząstki i antycząstki
- > Atom i cząsteczka
-
>
Związki metali przejściowych
- > Powłoka walencyjna metali przejściowych
- > Efekt Jahna-Tellera
- > Teoria pola krystalicznego
- > Teoria pola ligandów
- > Widma elektronowe
- > Wiązania metal-metal
- > Własności magnetyczne
- > Trwałość związków koordynacyjnych
- > Związki z ligandami π–akceptorowymi
- > Arenowe związki koordynacyjne
- > Oddziaływania agostyczne
- > Wiązania chemiczne
- > Pojęcia chemii nieorganicznej
- > Mechanizmy reakcji
- > Oddziaływania międzycząsteczkowe
- > Elementy fizyki
- > Chemia organiczna
 Grupa 17 – Fluorowce
Grupa 17 – Fluorowce
Fluor
Fluor to gazowy pierwiastek, niewiele cięższy od powietrza, trujący, o przenikliwym, silnie atakującym błonę śluzową, zapachu. Jest jedną z najbardziej reaktywnych substancji. Jako gaz charakteryzuje się zielonożółtym zabarwieniem. Skroplony i w fazie stałej uzyskuje jasnożółtą barwę. Jest najbardziej elektroujemnym pierwiastkiem: Jako gaz tworzy dwuatomowe cząsteczki o dość słabym wiązaniu pomiędzy atomami. Z prawie wszystkimi pierwiastkami tworzy związki, które zaliczają się do najbardziej trwałych. Jednym z najważniejszych związków fluoru jest fluorowodór (HF): silnie żrący kwas, trawiący wiele substancji m.in. szkło. W określonych warunkach fluor reaguje nawet z niektórymi gazami szlachetnymi tworząc fluorki helowców. Reakcje z większością metali przebiegają bardzo gwałtownie. Niektóre z nich (Al, Cu, Fe, Ni), tworzą na powierzchni ochronną warstwę fluorków blokującą dalsze trawienie. Metale te używa się do przechowywania tego pierwiastka. Niektóre jego związki są bardzo toksyczne. Znany (choć jego istnienie jest jeszcze dyskutowane) jest jeden kwas tlenowy fluoru HOF.
Fluor występuje w dość dużych ilościach w skorupie ziemskiej. Jest najbardziej rozpowszechnionym fluorowcem. W przyrodzie spotyka się go głównie w postaci fluorytu (CaF2), a także jako apatyt (Ca5(PO)4·3(OH,F) lub kriolit Na3AlF6. Jest także składnikiem organizmów żywych, u zwierząt jest ważnym składnikiem kości i zębów (około 0,3%). Zawartość w skorupie ziemskiej 0,0625% wagowego.
Otrzymywanie fluoru metodami czysto chemicznymi jest bardzo trudne ze względu na jego reaktywność. Podstawowymi używanymi metodami są metody elektrochemiczne. Najczęściej spotykaną jest metoda elektrochemicznego utleniania jonów fluorkowych F–. Wykorzystuje się w tym celu specjalne elektrolizery, odporne na działanie fluoru.
W przemyśle używa się wielu organicznych i nieorganicznych związków fluoru. Freony, (fluorowcopochodne węglowodorów) wykorzystywane były jako wypełniacze rozpylaczy aerozolowych oraz jako chłodziwo w lodówkach. Po odkryciu niszczącego wpływu tych substancji na ochronną warstwę ozonu atmosferycznego, praktycznie zaniechano ich stosowania. Inną substancją, w skład której wchodzi fluor, jest teflon. Jest on bardzo odporny chemicznie i termicznie, dlatego znalazł zastosowanie w przemyśle motoryzacyjnym jako materiał na uszczelki i wyposażenie wewnętrzne samochodów, a także jako wewnętrzna warstwa takich artykułów gospodarstwa domowego, jak np. patelnie czy kuchenki. W ostatnich dziesięcioleciach powstało wiele związków fluoru o przydatnych, a czasami bardzo unikalnych, właściwościach. Kluczowym związkiem w chemii fluoru jest fluorowodór (HF). Można z niego otrzymać praktycznie wszystkie związki fluoru. Poza syntezą używa się go również do trawienia szkła oraz jako katalizatora w syntezie wysokooktanowych benzyn. Fluorek uranu (VI) (UF6), gazowy związek uranu, znalazł zastosowanie głównie do rozdzielania izotopów tego promieniotwórczego pierwiastka. Niektóre związki fluoru dodawane w niewielkich ilościach do past do zębów i wody pitnej zapobiegają chorobom zębów. Pierwiastek ten oraz niektóre jego związki są wysoko toksyczne.
Związki fluoru:
kwas fluorowodorowy – HF – wodny roztwór fluorowodoru jest bezbarwną cieczą o ostrej woni. Stężony kwas zawiera około 40% HF. Tworzy z wodą mieszaninę azeotropową o temperaturze wrzenia 393K i stężeniu 35,4%. Kwas fluorowodorowy rozpuszcza większość metali oprócz złota, platyny i ołowiu. Jest trujący, wywołuje trudno gojące się rany. Pod wpływem tego kwasu (lub gazowego fluorowodoru) krzemionka SiO2, tak wolna jak i związana w krzemianach, ulega przemianie w łatwo lotny SiF4. Dlatego kwas fluorowodorowy znajduje zastosowanie do trawienia szkła. Ponadto wykazuje działanie bakteriobójcze, dlatego jego rozcieńczonych roztworów używa się do celów dezynfekcyjnych (przemysł drożdżowy).
kwas fluorowy – HOF – ze względu na dużą elektroujemność fluoru wiązanie tlen-fluor w tym związku jest spolaryzowane w ten sposób, że tlen formalnie znajduje się na 0 stopniu utlenienia. W temperaturze pokojowej kwas ten jest nietrwały, a okres rozkładu jest krótszy od 1 godziny. Otrzymano go po raz pierwszy w 1971 roku przepuszczając fluor nad lodem. Topi się w temperaturze 156K. W reakcji z wodą (otrzymywany nad lodem) powstaje HF, O2, H2O2. W warunkach ostrożnej hydrolizy tworzy tylko HF i nadtlenek wodoru. Sole tego kwasu nie są znane, ale znane są związki typu R-O-F, gdzie R = SF5, SeF5, ClO3, NO2, CF3, CF3CO, FSO2.
| Konfiguracja elektronowa | He 2s2p5 | |
| Masa atomowa | 18,99 | |
| Gęstość [kg·m–3] | 1,696 (273K) | |
| Główny stopień utlenienia | -1 | |
| Izotopy | masa - zawartość - okres półrozpadu | |
| 18F 19F |
0% - 109,7 minut 18,988 - 100% - stabilny |
|
| Temperatura topnienia [K] | 53,5 | |
| Temperatura wrzenia [K] | 85,0 | |
| Promień atomowy [pm] | 70,9 | |
| Powinowactwo elektronowe [kJ·mol–1] | 328 | |
| Energia jonizacji [kJ·mol–1] | 1681 F → F+ 3374 F+ → F2+ 6050 F2+ → F3+ |
|
| Elektroujemność (Pauling) | 3,98 | |
| Energia wiązań kowalencyjnych [kJ·mol–1] | F-F F-O F-N |
159 190 272 |
Chlor
Chlor jest żółto-zielonym, 2,5 razy cięższym od powietrza silnie trującym gazem o przenikliwym, duszącym zapachu. Daje się łatwo skroplić, łatwo rozpuszcza się w wodzie (woda chlorowa). Jest bardzo reaktywnym pierwiastkiem, nie występującym w naturze w wolnej postaci. Reaguje już w temperaturze pokojowej, a po podgrzaniu reakcje z nim mają często gwałtowny, egzotermiczny przebieg. W stosunku do tlenu, azotu węgla i gazów szlachetnych (tylko ksenon), zachowuje się biernie, ale pośrednimi metodami można uzyskać związki chloru z tymi pierwiastkami. Reaktywność chloru znacznie wzrasta, gdy jest on zawilgocony, tworzy wówczas chlorek nawet ze złotem (AuCl3). Z wodorem tworzy chlorowodór (HCl), w roztworze wodnym nazywany kwasem solnym. Reakcja ta, katalizowana energią światła, jest silnie egzotermiczna, a nawet wybuchowa. Chlor ma silną tendencję do łączenia się z wodorem, odbierając go innym związkom. Jego trujące właściwości zostały "wykorzystane" w czasie I wojny światowej (gaz bojowy).
Tlenki chloru występują na stopniach utleniania od-1 przez +3, +4, +6 do +7. Tworzy też szereg kwasów tlenowych. Wolny chlor nie występuje w naturze. Największe ilości tego niemetalu, w postaci jonów chlorkowych (Cl–), zawarte są w wodzie morskiej. Szacuje się, że sól, powstała z wyparowania całej wody morskiej, pokryłaby powierzchnię lądów warstwą o grubości 100 m. Wyparowana dawniej woda morska tworzy dzisiejsze pokłady soli kamiennej będącej mieszaniną: soli kuchennej (NaCl), chlorku magnezu (MgCl2) i potasu (KCl). Chlorki te otrzymuje się metodami górniczymi z pokładów soli lub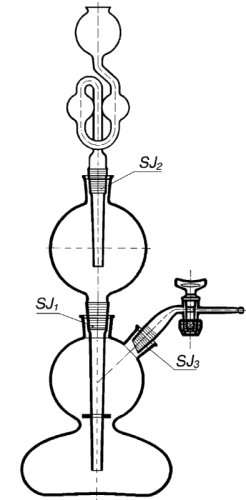 Aparat Kippa odparowując wodę morską. Zawartość w skorupie ziemskiej 0,1% wagowy. W laboratorium otrzymuje się chlor przez utlenienie stężonego kwasu solnego tlenkiem manganu(IV) (MnO2) lub manganianem(VII) potasu (KMnO4). Można również wykorzystać reakcję wapna chlorowanego (CaCl(OCl)) z kwasem solnym w aparacie Kippa. Technicznie otrzymuje się go najczęściej poprzez elektrolizę wodnych roztworów chlorku sodowego (soli kuchennej). Chlor jest kluczowym produktem nieorganicznego przemysłu chemicznego, a zapotrzebowanie na niego stale wzrasta. Zastosowanie chloru i chloranów to bielenie (przemysł papierniczy, celulozowy) i odkażanie (ziarno, woda, ścieki). Związki tego pierwiastka są również ważnym półproduktem i odczynnikiem w syntezie innych, organicznych i nieorganicznych substancji (fenole, insektycydy, DDT, freony). Wodne roztwory pochodnych i samego chloru stosowane są powszechnie w gospodarstwie domowym. Przy używaniu tych substancji należy zachować szczególną ostrożność.
Aparat Kippa odparowując wodę morską. Zawartość w skorupie ziemskiej 0,1% wagowy. W laboratorium otrzymuje się chlor przez utlenienie stężonego kwasu solnego tlenkiem manganu(IV) (MnO2) lub manganianem(VII) potasu (KMnO4). Można również wykorzystać reakcję wapna chlorowanego (CaCl(OCl)) z kwasem solnym w aparacie Kippa. Technicznie otrzymuje się go najczęściej poprzez elektrolizę wodnych roztworów chlorku sodowego (soli kuchennej). Chlor jest kluczowym produktem nieorganicznego przemysłu chemicznego, a zapotrzebowanie na niego stale wzrasta. Zastosowanie chloru i chloranów to bielenie (przemysł papierniczy, celulozowy) i odkażanie (ziarno, woda, ścieki). Związki tego pierwiastka są również ważnym półproduktem i odczynnikiem w syntezie innych, organicznych i nieorganicznych substancji (fenole, insektycydy, DDT, freony). Wodne roztwory pochodnych i samego chloru stosowane są powszechnie w gospodarstwie domowym. Przy używaniu tych substancji należy zachować szczególną ostrożność.
Związki chloru:
woda chlorowa – nasycony roztwór chloru w wodzie zawierający 4,6g Cl2 w 1 obj. wody, stosowany jako energiczny utleniacz w laboratoriach chemicznych i przemyśle. Woda chlorowa nie jest roztworem w sensie fizycznym, gdyż zachodzące tu reakcje prowadzą do powstania równowagi:
Cl2 + H2O ↔ HCl + HClO
Obecność kwasów solnego i podchlorawego nadaje roztworowi odczyn kwaśny. Na świetle następuje rozkład HClO:
2HClO → 2HCl + O2
i woda chlorowa traci swe własności utleniające.
chlorowodór – HCl – bezbarwny gaz dymiący w wilgotnym powietrzu o ostrej, duszącej woni. Cięższy od powietrza, niepalny. Temperatura wrzenia –85°C; temperatura topnienia –112°C. W wodzie rozpuszcza się bardzo dobrze w wydzieleniem ciepła i utworzeniem kwasu solnego. Suchy chlorowodór jest znacznie mniej aktywny od kwasu solnego. Otrzymywany przez działanie kwasem siarkowym(VI) na sól kamienną (NaCl) lub w wyniku bezpośredniej syntezy z pierwiastków. Głownie stosowany do otrzymywania kwasu solnego i w niektórych syntezach organicznych.
kwas solny – HCl – roztwór chlorowodoru w wodzie. Bezbarwna ciecz, dymiąca na powietrzu. Stężony kwas solny zawiera około 38% HCl i ma gęstość 1,19 g·cm–3. Zależność stężenia od gęstości w przypadku kwasu solnego ma pewną charakterystyczną cechę. Otóż dwie cyfry po przecinku z gęstości kwasu pomnożone przez dwa dają stężenie roztworu kwasu. Otrzymywany przez pochłanianie gazowego chlorowodoru w wodzie. Techniczny kwas solny ma zabarwienie żółte ze względu na obecność żelaza. Znajduje zastosowanie do ekstrakcji rud metali, do trawienia metali, lutowania, scukrzania drewna, w syntezach organicznych, w ceramice.
tlenki chloru –
Cl2O – żółtobrązowy gaz, otrzymywany w wyniku przepuszczania chloru na d tlenkiem rtęci(II):
2Cl2 + 2HgO → HgCl2·HgO + Cl2O
W obecności reduktorów ten tlenek może eksplodować. Jego cząsteczka ma budowę trójkąta. Z zasadami tworzy podchloryny.
ClO2 – żółty gaz otrzymywany w warunkach laboratoryjnych działaniem stężonego kwasu siarkowego(VI) na KClO3 w temperaturze 0°C. Jest substancją o silnych własnościach utleniających nietrwałą ulegającą rozpadowi nawet pod wpływem słabego ogrzania. Z roztworami zasad tworzy mieszaninę chloranów(III) i chloranów(V):
2ClO2 + 2NaOH → NaClO2 + NaClO3 + H2O
Cl2O6 – powstaje w reakcji pomiędzy ozonem i ClO2 w temperaturze 0°C. Jest ciemnoczerwoną cieczą, wykazującą silne własności utleniające. Z zasadami dysproporcjonuje dając chlorany(V) i chlorany(VII):
Cl2O6 + 2NaOH → NaClO3 + NaClO4 + H2O
Cl2O7 – bezbarwna ciecz powstająca przy odwadnianiu kwasu chlorowego(VII) (HClO4) tlenkiem fosforu(V). Jest bezwodnikiem kwasu chlorowego(VII).
kwasy tlenowe chloru – z istniejących kwasów tlenowych chloru część występuje tylko w postaci soli.
kwas chlorowy(I) – HClO – daje się otrzymać tylko w postaci rozcieńczonych roztworów przez wprowadzenie chloru do wodnej zawiesiny tlenku rtęci(II):
2Cl2 + 2HgO + H2O → HgO·HgCl2 + 2HClO
Jest kwasem nietrwałym ulegającym rozkładowi podczas zagęszczania roztworu. Sole tego kwasu są trwałe. Otrzymuje się je przez wprowadzenie chloru do roztworu zasady. Chlorany(I) są wykorzystywane jako środki bielące i dezynfekujące.
kwas chlorowy(III) – HClO2 – można go otrzymać jedynie w postaci rozcieńczonego roztworu. Jest kwasem mocniejszym od chlorowego(I). Podobnie jak jego sole jest silnym utleniaczem.
kwas chlorowy(V) – HClO3 – istnieje tylko w roztworach. Jest kwasem silnym o własnościach utleniających. Sole tego kwasu otrzymuje się w wyniku dysproporcjonowania chloranów(I). Chlorany(V) zmieszane z substancjami łatwo się utleniającymi wybuchają podczas ogrzania.
kwas chlorowy(VII) – HClO4 – należy do najmocniejszych znanych kwasów. Jest bardzo silnym środkiem utleniającym. W temperaturze pokojowej jest bezbarwną, oleistą cieczą, łatwo wybuchającą w czasie ogrzewania lub w obecności substancji organicznych. Otrzymuje się go w wyniku działania kwasu siarkowego(VI) na chlorany(VII).
| Konfiguracja elektronowa | Ne 3s23p5 | |
| Masa atomowa | 35,453 | |
| Gęstość [kg·m–3] | 3,214 (273K) | |
| Główny stopień utlenienia | -1; +7 (+1; +3; +4; +6) | |
| Izotopy: | masa - zawartość - okres półrozpadu | |
| 35Cl 36Cl 37Cl |
34,969 - 75,77% - stabilny 35,980 - 0% - 3,1×105 lat 36,966 - 24,23% - stabilny |
|
| Temperatura topnienia [K] | 172,1 | |
| Temperatura wrzenia [K] | 238,5 | |
| Promień atomowy [pm] | 181 Cl– | |
| Powinowactwo elektronowe [kJ·mol–1] | 349,0 | |
| Energia jonizacji [kJ·mol–1] | 1251,1 Cl → Cl+ 2297 Cl+ → Cl2+ 3826 Cl2+ → Cl3+ |
|
| Elektroujemność (Pauling) | 3,16 | |
| Energia wiązań kowalencyjnych [kJ·mol–1] | Cl-O Cl-Cl Cl-F |
206 242 257 |
Brom
Brom w warunkach normalnych jest trującą, łatwo parującą czerwonobrunatną cieczą. Cięższe od powietrza, posiadające charakterystyczny zapach pary bromu są dwuatomowymi cząsteczkami powodującymi ostre zapalenie błon śluzowych. Ciekły brom powoduje powstawanie bolesnych, trudno gojących się ran na skórze. Jest obok rtęci jednym z dwóch pierwiastków występujących w postaci płynnej w pokojowej temperaturze.
Jego reakcje przypominają chlor, lecz jest on mniej aktywny. Tworzy związki z większością pierwiastków, lecz reakcje te nie są tak gwałtowne jak w przypadku chloru. Zaskakującym faktem jest to, że pierwiastek ten reaguje z sodem bardzo powoli i po podgrzaniu, a reakcja z potasem przebiega bardzo gwałtownie. Z wodorem tworzy HBr. Brom tworzy związki z innymi halogenkami (chlor i fluor), a z tlenem kwasy tlenowe (HBrO, HBrO2, HBrO3, HBrO4) i tlenki. Ze złotem tworzy bromek złota (AuBr3). Chlorowiec ten nieznacznie rozpuszcza się w wodzie, a roztwór taki nosi nazwę wody bromowej.
Brom występuje bardzo szeroko w przyrodzie, a największym rezerwuarem jonów bromkowych jest, pomimo stosunkowo małego stężenia, ocean. Pierwiastek ten towarzyszy także chlorowi w jego złożach soli. Nie występuje w stanie wolnym. Zawartość w skorupie ziemskiej 0,00025% wag.
W przemyśle otrzymuje się go głównie z wody morskiej, dzięki metodzie składającej się z następujących etapów:
- utlenienie jonów bromkowych gazowym chlorem i wydzielenie gazowego bromu z roztworu (oddzielenie od jonów chlorkowych),
- ponowne wprowadzenie do roztworu w postaci jonów (roztwór czysty, bez jonów chlorkowych), - zakwaszenie kwasem siarkowym i destylacja. W laboratorium uzyskuje się go poprzez wprowadzenie silnego utleniacza (KMnO4, MnO2, stęż. H2SO4) do roztworu, w którym są jony bromkowe.
Zapotrzebowanie na brom jest o wiele mniejsze niż na chlor. Stosuje się go w środkach gaśniczych (składnik freonów). Używa się go również do otrzymywania barwników i pestycydów. Jest składnikiem wielu leków. Dużą część produkowanego bromu zużywa się do produkcji bromku etylu (dibromoetanu (C2H4Br)) dodawanego do paliwa samochodowego jako środka przeciwstukowego. Fluorki bromu (BrF3 i BrF5) stosuje się do fluorowania. Bromiany(V) i (VII) są odczynnikami w chemii analitycznej.
Związki bromu:
bromowodór – HBr – bezbarwny gaz o temperaturze wrzenia -67°C i duszącej woni. Ma własności redukujące. Łatwo rozpuszczalny w wodzie 600 objętości HBr rozpuszcza się w 1 obj. wody o temperaturze 0°C tworząc mocny kwas. Solami tego kwasu są bromki. Otrzymywany z bromków metali pod wpływem kwasów nieutleniających lub przez hydrolizę bromków niemetali; przez redukcję wody bromowej siarkowodorem:
Br2·aq + H2S → 2HBr + S
Znajduje zastosowanie do otrzymywania bromków metali i w laboratoriach do syntez organicznych.
tlenki bromu –
Br2O – powstaje w wyniku przepuszczania par bromu nad świeżo otrzymanym HgO. Jest trwały tylko do temperatury 223K, jako ciemnobrunatna substancja stała. W temperaturze około 255K topi się z rozkładem.
BrO2 – powstaje podczas utleniania bromu ozonem. W temperaturach niższych od 233K jest jasnożółtą substancją stałą. Powyżej tej temperatury rozkłada się na pierwiastki.
halogenki bromu –
BrF – jasnoczerwony gaz o temperaturze wrzenia 293K i topnienia 240K. Daje się otrzymać bezpośrednio z pierwiastków. Bardzo łatwo dysproporcjonuje do Br2 i BrF3.
BrF3 – powstaje w wyniku bezpośredniej syntezy z pierwiastków w temperaturze 473K. Jest bezbarwną cieczą o temperaturze wrzenia 399K i krzepnięcia 282K. Wykazuje znaczne przewodnictwo elektryczne co wskazuje na daleko posuniętą autodysocjację.
BrF5 – bezbarwna ciecz o temperaturze wrzenia 314K i topnienia 213K. Otrzymywany w reakcji bromu z fluorkiem bromu(III).
BrCl – otrzymuje się przez zmieszanie chloru z bromem. Już w temperaturze pokojowej jest on zdysocjowany w 9% na wolne fluorowce. Występuje jako czerwonożółta ciecz o temperaturze krzepnięcia 219K. Temperatury wrzenia nie daje się wyznaczyć ze względu na rozkład związku.
kwasy tlenowe bromu – z istniejących kwasów tlenowych bromu część występuje tylko w postaci soli.
kwas bromowy(I) – HBrO – daje się otrzymać tylko w postaci rozcieńczonych roztworów przez wprowadzenie bromu do wodnej zawiesiny tlenku rtęci(II):
2Br2 + 2HgO + H2O → HgO·HgBr2 + 2HBrO
Jest kwasem nietrwałym ulegającym rozkładowi podczas zagęszczania roztworu. Sole tego kwasu są trwałe. Otrzymuje się je przez wprowadzenie bromu do roztworu zasady. Bromiany(I) ulegają podczas ogrzewania dysproporcjonowaniu z utworzeniem bromianów(V) i bromków:
3NaBrO → NaBrO3 + 2NaBr
kwas bromowy(V) – HBrO3 – też można otrzymać jedynie w postaci rozcieńczonego roztworu. Jest kwasem mocnym. Podobnie jak jego sole jest silnym utleniaczem. o własnościach utleniających podobnie jak jego sole.
kwas bromowy(VII) – HBrO4 – powstaje w wyniku utleniania bromianów(V) silnymi utleniaczami jak fluor lub fluorek ksenonu. Istnieje tylko w roztworze; jest silnym kwasem.
woda bromowa – nasycony roztwór wodny bromu zawierający 3,6g Br2 rozpuszczonego w 100g wody. Stosowany w laboratoriach i przemyśle jako utleniacz. W wodzie bromowej przebiegają reakcje prowadzące do utworzenia HBr i HBrO. HBrO powoli rozkłada się z utworzeniem HBr i tlenu.
| Konfiguracja elektronowa | Ar 3d104s24p5 |
| Masa atomowa | 79,904 |
| Izotopy | 79Br (50,69%); 81Br (49,31%) |
| Temperatura topnienia | 265,95K |
| Temperatura wrzenia | 331,93K |
| Promień atomowy [pm] | 196 (Br–) |
| Powinowactwo elektronowe [kJ·mol–1] | 324,7 |
| Energia jonizacji [kJ·mol–1] | 1139,9 Br → Br+ 2104 Br+ → Br2+ 3500 Br2+ → Br3+ |
| Elektroujemność (Pauling) | 2,96 |
Jod
Reaktywny chemicznie chlorowiec. Jod, w odróżnieniu od innych chlorowców, jest ciałem stałym w pokojowej temperaturze. Jest połyskliwą, niebiesko-czarną substancją sublimującą po podgrzaniu i dającą fioletowe opary o drażniącym zapachu. Pary te łatwo można zestalić w procesie resublimacji na chłodnej powierzchni. W czystej postaci jod jest trujący. W naturze występuje tylko jeden trwały jego izotop. Jest, tak jak inne chlorowce, bardzo reaktywny. Słabo rozpuszcza się w wodzie, ale jest dobrze rozpuszczalny w wodnym roztworze jodku potasu (KI). Rozpuszcza się także w alkoholach, chloroformie i innych organicznych rozpuszczalnikach. Tworzy bogatą rodzinę związków, w których występuje na wielu stopniach utlenienia. Najchętniej reaguje z metalami tworząc jodki, z niemetalami reakcje przebiegają wolniej. Z wodorem tworzy jodowodór. Tworzy halogenki, kwasy tlenowe i tlenki.
Jod jest stosunkowo słabo rozpowszechnionym pierwiastkiem. Woda morska zawiera jego duże ilości. Znaczne ilości jodu występują również w tkankach roślin morskich - brunatnic. Na lądzie jego duże ilości występują m.in. w Chile, towarzysząc saletrze chilijskiej. Zawartość w skorupie ziemskiej 5·10–6% wag.
Otrzymywany jest głównie jako produkt uboczny procesu oczyszczania saletry chilijskiej. Jod to ważny mikroelement naszych organizmów, w których występuje jako składnik hormonów (hormon wzrostu). Brak jodu powoduje zaburzenia wzrostu i działalności tarczycy. W medycynie jod i jego alkoholowe roztwory (jodyna) wykorzystuje się do dezynfekcji. Używany jest także w fotografice i do produkcji barwników. Izotopy promieniotwórcze jodu znalazły zastosowanie w nauce, szczególnie w medycynie. Związki tego pierwiastka stosowane są także jako silne utleniacze.
Związki jodu:
jodki – związki zawierające jod na -1 stopniu utlenienia. Jodki niemetali powstają głównie w wyniku bezpośredniej syntezy. Jodki metali są solami kwasu jodowodorowego. Zazwyczaj są ciemniej zabarwione od analogicznych chlorków. Do ważniejszych jodków można zaliczyć:
jodek potasowy – KJ – bezbarwne ciało stałe; stosowany w fotografice, lecznictwie, chemii analitycznej (jodometria), syntezach innych jodków;
jodek srebra – AgI – żółty, znajduje zastosowanie w przemyśle fotograficznym;
jodek rtęci(II) – HgI2 - koralowoczerwony, rozpuszcza się w nadmiarze jodków z utworzeniem bezbarwnego jonu kompleksowego [HgJ4]2– (odczynnik Nesslea)
jodek ołowiu(II) – PbI2 - złocistożółty, rozpuszczalny w gorącej wodzie;
jodków miedzi(II) i żelaza(III) nie daje się otrzymać na skutek redukujących własności jonu jodkowego - powstają jodki miedzi(I) i żelaza(II).
jodowodór – HI – bezbarwny gaz o temperaturze wrzenia –50°C i duszącej woni. Jest mocnym reduktorem. W wodzie rozpuszcza się dobrze 425 obj. HI rozpuszczają się w 1 obj. wody w temperaturze 10°C tworząc mocny kwas.
fluorek jodu(I) – IF – wykryty metodami spektroskopowymi, w temperaturze pokojowej, w ilościach śladowych. Ulega dysproporcjonacji do I2 i IF5.
fluorek jodu(III) – IF3 – otrzymuje się jako żółty proszek w reakcji jodu z fluorem w atmosferze freonu w temperaturze 195K. Do temperatury 238K jest trwały, a powyżej dysproporcjonuje na I2 i IF5.
fluorek jodu(V) – IF5 – trwały w temperaturze pokojowej; temperatura topnienia 283K, wrzenia 374K. Otrzymywany w reakcji fluoru z nadmiarem jodu w lekko podwyższonej temperaturze. Ma zdolności do autojonizacji:
2IF5↔ IF4+ + IF6–
IF7 - powstaje w reakcji jodu w temperaturze 523-543K z nadmiarem fluoru; wrze w temperaturze 550K, topi się w 279,8K. W temperaturze pokojowej jest bezbarwnym gazem sublimującym w temperaturze 277,8K. Bardzo czuły na wilgoć, przez co jest zanieczyszczony IOF5.
chlorek jodu(I) – ICl – powstaje w reakcji ciekłego chloru z równoważną ilością jodu w postaci rubinowoczerwonych igieł o temperaturze topnienia 300,5K i wrzenia 370,3K.
chlorek jodu(III) –ICl3 - otrzymywany podczas chlorowania jodu nadmiarem chloru w postaci pomarańczowego proszku. Pod ciśnieniem 16MPa topi się w temperaturze 284K.
bromek jodu(I) – IBr – czerwonobrunatna substancja stała, powstająca w wyniku zmieszania pierwiastków; temperatura topnienia 309K, wrzenia 389K. W stanie pary jest silnie zdysocjowany na pierwiastki.
tlenki jodu –
I2O4 – otrzymuje się w wyniku reakcji gorącego kwasu siarkowego(VI) z kwasem jodowym(V). Jest żółtym ciałem stałym, które w wyniku ogrzewania powyżej 373K rozkłada się na I2O5 i I2. W zimnej wodzie rozpuszcza się słabo, w gorącej rozpuszcza się z utworzeniem kwasu jodowego(V) i jodu.
I2O5 – otrzymywany przez odwodnienie kwasu jodowego(V). w temperaturze około 573K rozkłada się na pierwiastki. Białe ciało stałe, o temperaturze topnienia 523K.
I2O7 – otrzymuje się jako polimeryczną substancję stałą o barwie pomarańczowej w reakcji dymiącego kwasu siarkowego(VI) z HIO4.
IOF3 – powstaje w reakcji fluorku jodu(V) z pentatlenkiem dijodu. Substancja stała ulegająca w temperaturze 383K rozkładowi na IO2F i IF5.
IO2F – powstaje w wyniku termicznego rozkładu IOF3 w temperaturze 383K.
IOF5 – powstaje w reakcji IF7 z wodą, krzemionką lub pentatlenkiem dijodu.
IO2F3 – otrzymywany w reakcji ortonadjodanu baru z kwasem fluorosulfonowym:
Ba3H4(IO6)2 + 14HSO3F → HOIOF4 + 8H2SO4 + 3Ba(SO3F)2
HOIOF4 + SO3 → IO2F3 + HSO3F
tlenowe kwasy jodu –
kwasy jodowy(I) – HIO – otrzymuje się podczas wytrząsania jodu z wodną zawiesiną HgO. Kwas nietrwały, dysproporcjonujący do jodu i kwasu jodowego(V) HIO3. Sole tego kwasu są trwalsze, ale też dysproporcjonują do jodku i jodanu(V) IO3–.
kwasy jodowy(V) – HIO3 – otrzymuje się przez utlenienie jodu stężonym kwasem azotowym(V), lub przez utlenienie jodu chlorem. Bezbarwna substancja krystaliczna; silny utleniacz.
kwasy jodowy(VII) –HIO4 – w stanie wolnym znany jako związek uwodniony H5IO6. Otrzymuje się go prze anodowe utlenienie kwasu jodowego(V); występuje jako bezbarwne, rozpływające się w powietrzu kryształy. Topi się w temperaturze 403K odszczepiając wodę i tlen i przechodząc w tlenek jodu(V).
| Konfiguracja elektronowa | Kr 4d105s2p5 | |
| Masa atomowa | 126,90447 | |
| Gęstość [kg×m3] | 4930 (293K) | |
| Główny stopień utlenienia | -1 (0; +3; +5; +7) | |
| Izotopy: | masa - zawartość - okres półrozpadu | |
| 123I 125I 127I 129I 131I |
0% - 13,3 godz. 0% - 60,2 dni 126,9 - 100% - stabilny 0% - 1,7·107 lat 0% - 8 dni |
|
| Temperatura topnienia [k] | 386,66 | |
| Temperatura wrzenia [K] | 457,51 | |
| Promień atomowy [pm] | 220 (I–) | |
| Powinowactwo elektronowe [kJ·mol–1] | 259,2 | |
| Energia jonizacji [kJ·mol–1] | 1008,4 I → I+ 1845,9 I+ → I2+ 3200 I2+ → I3+ |
|
| Elektroujemność (Pauling) | 2,66 | |
| Energia wiązań kowalencyjnych [kJ·mol–1] | I-H I-C I-O I-F I-Cl I-I I-Si I-P |
299 218 234 280 208 151 234 184 |
Astat
Astat jest radioaktywnym pierwiastkiem należącym do grupy chlorowców. Wytworzony został w 1940 roku w Stanach Zjednoczonych (D.R. Corson). Początkowo nazywano go alabamitem (od stanu Alabama), później zmieniono jego nazwę na astat (grec. astatos – niestabilny). Wszystkie jego izotopy są promieniotwórcze i mają bardzo krótki czas połowicznego rozpadu. Najtrwalsze z nich to: 210At (czas połowicznego rozpadu około 8 godzin) i 211At (około 7 godzin). Udało się wytworzyć izotopy astatu o masach atomowych od 200 do 219. Pierwiastek ten wykazuje cechy metalu. Jest silnie rakotwórczy. Nie występuje w naturze. Wyprodukowany w 1940 roku poprzez bombardowanie bizmutu cząstkami alfa. Wykorzystywany do celów czysto naukowych.
| Konfiguracja elektronowa | [Xe]4f145d106s26p5 | |
| Masa atomowa | 210 | |
| Główny stopień utlenienia | +1; +3 | |
| Izotopy: | masa - zawartość - okres półrozpadu | |
| 210At 211At |
0% - 8,3 godz. 210,99 - 0% - 7,21 godz.. |
|
| Temperatura topnienia [K] | 575 | |
| Temperatura wrzenia [K] | 610 | |
| Energia jonizacji [kJ·mol–1] | At → At+ 930 At+ → At2+ 1600 At2+ → At3+ 2900 |
|
| Powinowactwo elektronowe [kJ·mol–1] | 256 | |
| Energia wiązań kowalencyjnych [kJ·mol–1] | At–At | 110 |